Versión 1 - 25/10/2024
En adultos con sepsis o choque séptico, la administración de betalactámicos en infusión prolongada (>2 horas), comparado con bolos intermitentes convencionales (<2 horas), reduce la mortalidad en la UCI y por todas las causas a 90 días, sin diferencias en eventos adversos entre las dos estrategias. Para evitar 1 muerte se tendrían que tratar entre 25 y 33 pacientes. Por tanto, se recomienda implementar en la práctica clínica la estrategia de infusión prolongada, según disponibilidad de personal y recursos como accesos vasculares y bombas de infusión.
Certeza en la evidencia: moderada por riesgo de sesgos ⨁ ⨁ ⨁ ◯
Otros mensajes claves:
- La infusión prolongada de betalactámicos aumentó la probabilidad de curación clínica.
- No se encontró beneficio en cuanto a curación microbiológica y días de estancia en la UCI.
Es importante saber lo que no se conoce:
- Dentro de la estrategia de infusión prolongada de betalactámicos (>2 horas), se desconoce si existe un efecto dosis-respuesta con relación al tiempo de administración (Ej. 4 horas vs 24 horas).
Antecedentes
Anualmente, más de 18 millones de personas en el mundo desarrollan sepsis, con una incidencia de 66 a 300 casos por 100,000 habitantes en países desarrollados (1). La mayoría de los casos se adquieren en la comunidad y están presentes en la admisión hospitalaria (2,3). A pesar de los avances en el tratamiento, alrededor de 5.3 millones de personas mueren cada año (mortalidad >30%) (4).
Las estrategias para reducir la mortalidad en estos pacientes se integran en protocolos de reanimación oportuna (3), resaltando la administración temprana de antibióticos. No obstante, debido a las alteraciones fisiológicas propias de la condición y las cointervenciones que modifican la farmacocinética, existe incertidumbre sobre la dosificación más apropiada de los antibióticos, específicamente la duración de la infusión (5-7).
Los antibióticos betalactámicos, tratamiento de primera línea para la sepsis y el choque séptico, tienen una actividad bactericida dependiente del tiempo. Esto significa que requieren superar concentraciones inhibitorias mínimas (MIC, por sus siglas en inglés) durante al menos el 40-70% del intervalo de dosificación (8). Este efecto ha dado lugar a la justificación biológica de que las infusiones prolongadas (continuas o intermitentes extendidas, >2 horas) de betalactámicos pueden ser más efectivas en comparación con la dosificación intermitente convencional, por alcanzar mayor tiempo de concentración sobre la MIC (9,10).
Varios estudios farmacocinéticos-farmacodinámicos han demostrado que las infusiones prolongadas logran exposiciones de betalactámicos asociadas con una máxima eliminación bacteriana de manera más consistente que las infusiones intermitentes (11). Sin embargo, sigue siendo incierto si los efectos de la infusión prolongada de betalactámicos, en comparación con la infusión intermitente convencional, impactan de manera favorable en desenlaces centrados en el paciente como mortalidad (12-17).
En un ensayo clínico publicado recientemente (18) (n=7202) no se encontraron diferencias en términos de mortalidad a 90 días (OR 0.91, IC95% 0.81-1.01, p=0.08) cuando se comparó la administración de betalactámicos en infusión continua (24 horas) con bolos intermitentes (30 minutos). Este Recado explora la evidencia sobre la eficacia y seguridad de la infusión prolongada de betalactámicos, comparada con infusión convencional, en sepsis o choque séptico.
Información en la que se basa este Recado
La estrategia de búsqueda incluyó los términos “critically ill patients”, “intensive care unit”, “sepsis”, “septic shock,” “betalactam”, “carbapenem”, “cephalosporin”, “monobactam”, “penicillin”, “continuous infusion”, “extended infusion”, “prolonged infusion”, “intermittent infusion” en las bases de datos Medline/Pubmed, Embase, Cochrane, delimitando como relevantes las revisiones sistemáticas (RS) y metaanálisis a partir de 2019. Se incluyeron referencias cruzadas y búsquedas adicionales en Consensus (19) y Elicit AI (20).
Luego de filtrar para RS se recuperaron los estudios de Kondo et al. (21), Li et al. (22), Zhao et al. (23), Lin et al. (24) y Abdul-Aziz et al. (25), de los cuales se seleccionó el último dado su rigor metodológico e inclusión de ensayos clínicos recientes.
En la revisión sistemática de Abdul-Aziz (25) se incluyeron experimentos que reclutaron a participantes adultos críticamente enfermos con sepsis o choque séptico. Estos estudios compararon la administración de infusiones prolongadas de uno o más betalactámicos (ya sea infusiones continuas o extendidas >2 horas) con infusiones intermitentes convencionales (<2 horas). El desenlace primario fue mortalidad a 90 días, mientras que los desenlaces secundarios incluyeron mortalidad en la UCI, tasa de curación clínica, curación microbiológica, y tiempo de estancia en la UCI.
Se preespecificaron 7 subgrupos para el desenlace primario:
- Administración de meropenem frente a piperacilina-tazobactam.
- Infección con cultivo positivo frente a infección con cultivo negativo.
- Infección por Gram negativos frente a Gram positivos.
- Necesidad o no de terapia de reemplazo renal.
- Infección pulmonar frente a otras infecciones.
- Sepsis frente a choque séptico.
- Participantes masculinos frente a femeninos.
Los metaanálisis en la RS se realizaron utilizando un enfoque bayesiano como el principal método de análisis, complementado por un análisis frecuentista como enfoque secundario. Para le evaluación crítica de los estudios primarios los autores emplearon la herramienta RoB 2 de Cochrane.
Resultados
La RS incluyó 18 ensayos clínicos aleatorizados (n=9108 participantes, 65% hombres, mediana de edad 57 años). Las medianas de APACHE II y SOFA fueron 20 (RIQ 18-22) y 8 (RIQ 6-11) puntos, respectivamente.
De los 18 ensayos, 17 compararon infusiones continuas de betalactámicos con infusiones intermitentes convencionales (<2 horas), mientras que 1 ensayo comparó infusiones intermitentes extendidas (>2 horas) con infusiones convencionales. Los antibióticos estudiados incluyeron meropenem (11 estudios), piperacilina-tazobactam (8 estudios), cefepime (3 estudios), así como como ticarcilina-clavulanato, amoxicilina-clavulanato, ampicilina-sulbactam, ceftriaxona e imipenem-cilastatina (1 ensayo cada uno).
La tabla 1 compara enfoques bayesianos y frecuentistas en un metaanálisis. Ambos enfoques muestran que la estrategia de infusión continua reduce el riesgo de muerte a 90 días, pero con diferencias en la magnitud del efecto y la incertidumbre. En el metaanálisis primario (bayesiano) se observa una reducción del 14% en el riesgo de muerte a 90 días. Esto quiere decir, en términos absolutos, que se requiere tratar entre 25 y 33 pacientes con infusión continua para evitar una muerte.
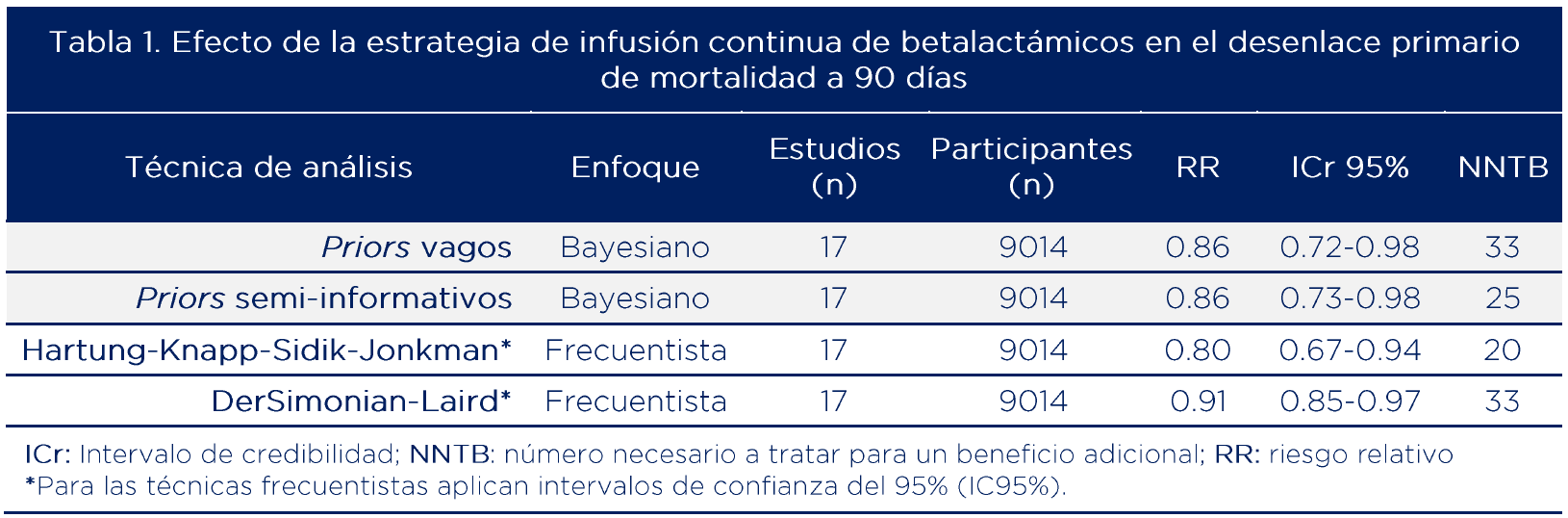
Nota metodológica:
La elección entre el enfoque frecuentista y bayesiano depende del contexto. El enfoque frecuentista, más común en la práctica, se basa solo en los datos observados y es útil con grandes conjuntos de datos, pero puede subestimar la incertidumbre en situaciones con pocos datos o alta variabilidad. Por otro lado, el enfoque bayesiano permite integrar información previa (priors) junto con los datos actuales, siendo más flexible y ofreciendo resultados más ajustados cuando los datos son limitados o heterogéneos, aunque su implementación es más compleja y depende de la correcta elección de los priors (26).
La tabla 2 muestra, a partir de un enfoque frecuentista, que al incluir el estudio BLING III (18) (71.5% del peso en el metaanálisis) se reduce la imprecisión, mejorando la certeza aunque con un menor tamaño del efecto. No obstante, este sigue siendo clínicamente importante en términos de mortalidad dado que el número necesario a tratar para un beneficio adicional (NNTB) es 33.
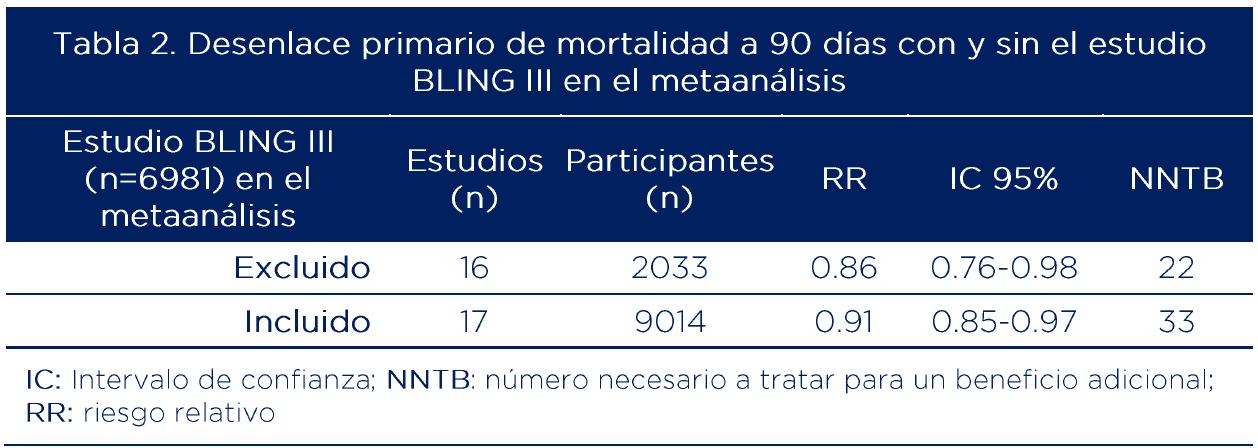
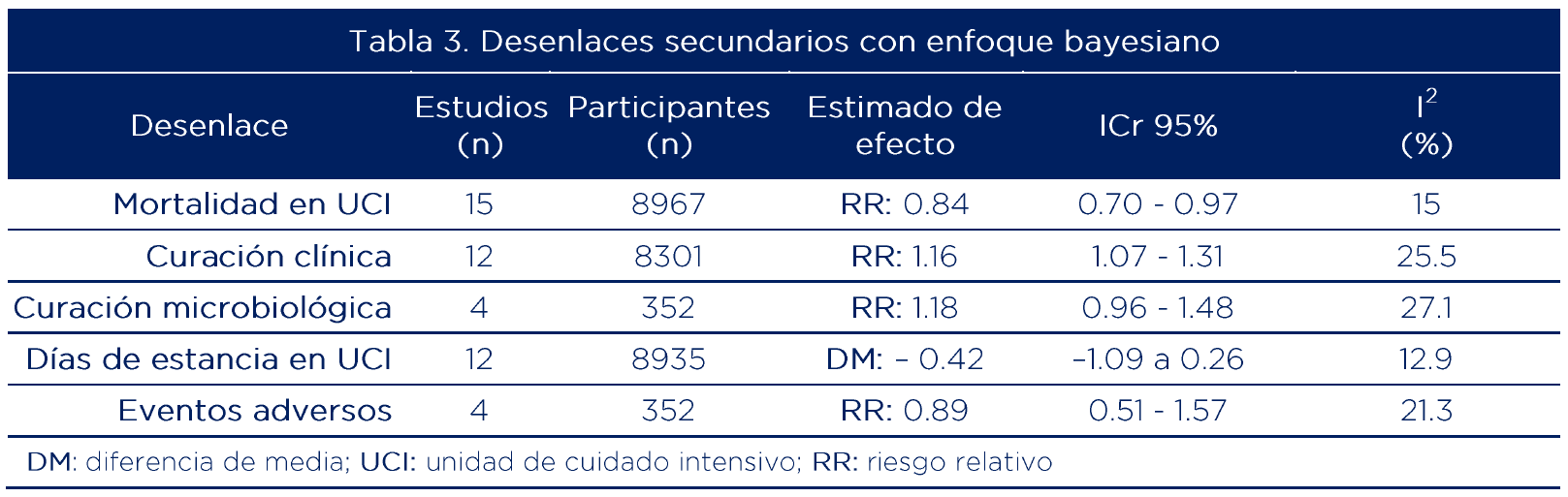
Los datos de la tabla 3 muestran que la estrategia de infusión prolongada comparada con la de infusión intermitente convencional, reduce el riesgo de muerte en la UCI y aumenta la probabilidad de curación clínica en un 16%. No se encontraron diferencias en las dos estrategias en cuanto a curación microbiológica, días de estancia en la UCI y eventos adversos. Esta última tendencia fue la misma en el análisis por subgrupos, donde no se encontró un efecto diferencial.
Información sobre la evidencia que soporta este Recado
Luego de aplicar la herramienta de evaluación crítica AMSTAR-2 (27) se concluyó confianza alta en la RS (anexo 1). A partir del instrumento RoB-2 de Cochrane, los autores de la RS, identificaron estudios con alto riesgo de sesgo en todos los desenlaces (28).
La certeza global en la evidencia establecida con la metodología GRADE (29) fue considerada moderada (por riesgo de sesgo) para los desenlaces críticos de mortalidad a 90 días y mortalidad en la UCI (anexo 2).
Unidad de Síntesis y Transferencia de Conocimiento | Correspondencia: udstransferencia@lacardio.org
Rodríguez, J*; Anderson Felipe Arias*; Jose D. Cruz-Cuevas**; Balcázar-Muñoz, AM**+; Romero-Orjuela SP**
(*)Desarrollo, (**)Edición, (+)Diseminación
¿Tienes una pregunta clínica que nuestra Unidad de Síntesis y Transferencia del Conocimiento pueda resolver a través de evidencia científica?
Sí, enviar pregunta
Referencias
Keeley A, Hine P, Nsutebu E. The recognition and management of sepsis and septic shock: a guide for non-intensivists. Postgrad Med J, 2017;93(1104):626-34. Disponible en: https://doi.org/10.1136/postgradmedj-2016-134519
Singer M, Deutschman C, Seymour C, Shankar- Hari M, Annane D, Bauer M, et al. The third international consensus definitions for sepsis and septic shock (sepsis-3). JAMA, 2016;35(8):801- 810. Disponible en :https://www.mendeley.com/ catalogue/third-international-consensus- definitions-sepsis-septic-shock-sepsis3/
Evans, L., Rhodes, A., Alhazzani, W., Antonelli, M., Coopersmith, C. M., French, C., Machado, F. R., Mcintyre, L., Ostermann, M., Prescott, H. C., Schorr, C., Simpson, S., Wiersinga, W. J., Alshamsi, F., Angus, D. C., Arabi, Y., Azevedo, L., Beale, R., Beilman, G., Belley-Cote, E., Levy, M. (2021). Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021. Intensive care medicine, 47(11), 1181–1247. https://doi.org/10.1007/s00134-021-06506-y
Fleischmann C, Scherag A, Adhikari NK, Hartog CS, Tsaganos T, Schlattmann P, Angus DC, Reinhart K. Assessment of Global Incidence and Mortality of Hospital-treated Sepsis. Current Estimates and Limitations. Am J Respir Crit Care Med. 2016;193(3):259-72. Disponible en: https://doi.org/10.1164/rccm.201504-0781oc vancuver
Roberts JA, Paul SK, Akova M, et al; DALI Study. DALI: defining antibiotic levels in intensive care unit patients: are current β-lactam antibiotic doses sufficient for critically ill patients? Clin Infect Dis. 2014;58(8):1072-1083. doi:10.1093/cid/ciu027
Roberts JA, Joynt GM, Lee A, et al; SMARRT Study Collaborators and the ANZICS Clinical Trials Group. The effect of renal replacement therapy and antibiotic dose on antibiotic concentrations in critically ill patients: data from the Multinational Sampling Antibiotics in Renal Replacement Therapy study. Clin Infect Dis. 2021;72(8):1369-1378. doi:10. 1093/cid/ciaa224
Shekar K, Abdul-Aziz MH, Cheng V, et al. Antimicrobial exposures in critically ill patients receiving extracorporeal membrane oxygenation. Am J Respir Crit Care Med. 2023;207(6):704-720. doi:10.1164/rccm.202207-1393OC
Craig WA. Pharmacokinetic/pharmacodynamic parameters: rationale for antibacterial dosing of mice and men. Clin Infect Dis. 1998;26(1):1-10. doi:10.1086/516284
Mouton JW, Vinks AA. Is continuous infusion of beta-lactam antibiotics worthwhile? efficacy and pharmacokinetic considerations.J Antimicrob Chemother. 1996;38(1):5-15. doi:10.1093/jac/38.1.5
Abdul-Aziz MH, Portunato F, Roberts JA. Prolonged infusion of beta-lactam antibiotics for gram-negative infections: rationale and evidence base. Curr Opin Infect Dis. 2020;33(6):501-510. doi:10.1097/QCO.0000000000000681
Dhaese S, Heffernan A, Liu D, et al. Prolonged versus intermittent infusion of β-lactam antibiotics: a systematic review and meta-regression of bacterial killing in preclinical infection models. Clin Pharmacokinet. 2020;59(10):1237-1250. doi:10.1007/s40262-020-00919-6 .
Roberts JA, Webb S, Paterson D, Ho KM, Lipman J. A systematic review on clinical benefits of continuous administration of beta-lactam antibiotics. Crit Care Med. 2009;37(6):2071-2078. doi:10.1097/CCM.0b013e3181a0054d
Roberts JA, Abdul-Aziz MH, Davis JS, et al. Continuous versus intermittent β-lactam infusion in severe sepsis: a meta-analysis of individual patient data from randomized trials. Am J Respir Crit Care Med. 2016;194(6):681-691. doi:10.1164/rccm.201601- 0024OC
Vardakas KZ, Voulgaris GL, Maliaros A, Samonis G, Falagas ME. Prolonged versus short-term intravenous infusion of antipseudomonal β-lactams for patients with sepsis: a systematic review and meta-analysis of randomised trials. Lancet Infect Dis. 2018;18(1):108-120. doi:10.1016/S1473-3099(17)30615-1
Kondo Y, Ota K, Imura H, Hara N, Shime N. Prolonged versus intermittent β-lactam antibiotics intravenous infusion strategy in sepsis or septic shock patients: a systematic review with meta-analysis and trial sequential analysis of randomized trials.J Intensive Care. 2020;8:77. doi:10.1186/s40560-020-00490-z
Li X, Long Y, Wu G, et al. Prolonged vs intermittent intravenous infusion of β-lactam antibiotics for patients with sepsis: a systematic review of randomized clinical trials with meta-analysis and trial sequential analysis. Ann Intensive Care. 2023;13(1):121. doi:10.1186/s13613-023-01222-w
Lokhandwala A, Patel P, Isaak AK, et al. Comparison of the effectiveness of prolonged infusion and intermittent infusion of meropenem in patients with sepsis: a meta-analysis. Cureus. 2023;15(10):e46990. doi:10.7759/cureus.46990.
Dulhunty JM, Brett SJ, De Waele J, et al. Continuous vs intermittent β-lactam antibiotic infusions in critically ill patients with sepsis: the BLING III randomized clinical trial.JAMA. Published online June 12, 2024. doi:10.1001/jama.2024.9779.
Consensus: AI Search Engine for Research. (s.f.). Consensus: AI-powered Academic Search Engine. https://consensus.app/search/
Elicit: The AI Research Assistant. (s.f.-a). Elicit: The AI Research Assistant. https://elicit.com/
Kondo Y, Ota K, Imura H, Hara N, Shime N. Prolonged versus intermittent β-lactam antibiotics intravenous infusion strategy in sepsis or septic shock patients: a systematic review with meta-analysis and trial sequential analysis of randomized trials. J Intensive Care. 2020 Oct 6;8:77. doi: 10.1186/s40560-020-00490-z.
Li X, Long Y, Wu G, Li R, Zhou M, He A, Jiang Z. Prolonged vs intermittent intravenous infusion of β-lactam antibiotics for patients with sepsis: a systematic review of randomized clinical trials with meta-analysis and trial sequential analysis. Ann Intensive Care. 2023 Dec 5;13(1):121. doi: 10.1186/s13613-023-01222-w
Zhao Y, Zang B, Wang Q. Prolonged versus intermittent β-lactam infusion in sepsis: a systematic review and meta-analysis of randomized controlled trials. Ann Intensive Care. 2024 Feb 18;14(1):30. doi: 10.1186/s13613-024-01263-9.
Lin CC, Wu JY, Huang PY, Sung HL, Tung YC, Lai CC, Wei YF, Fu PK. Comparing prolonged infusion to intermittent infusion strategies for beta-lactam antibiotics in patients with gram-negative bacterial infections: a systematic review and meta-analysis. Expert Rev Anti Infect Ther. 2024 Mar 5:1-11. doi: 10.1080/14787210.2024.2324940
Abdul-Aziz MH, Hammond NE, Brett SJ, Cotta MO, De Waele JJ, Devaux A et al. Prolonged vs Intermittent Infusions of β-Lactam Antibiotics in Adults With Sepsis or Septic Shock: A Systematic Review and Meta-Analysis. JAMA. 2024 Aug 27;332(8):638-648. doi: 10.1001/jama.2024.9803.
Moran JL, Linden A. Problematic meta-analyses: Bayesian and frequentist perspectives on combining randomized controlled trials and non-randomized studies. BMC Med Res Methodol. 2024 Apr 27;24(1):99. doi: 10.1186/s12874-024-02215-4
Shea BJ, Reeves BC, Wells G, Thuku M, Hamel C, Moran J, Moher D, Tugwell P, Welch V, Kristjansson E, Henry DA. AMSTAR 2: a critical appraisal tool for systematic reviews that include randomised or non-randomised studies of healthcare interventions, or both. BMJ. 2017 Sep 21;358:j4008. doi: 10.1136/bmj.j4008
Sterne JAC, Savović J, Page MJ, Elbers RG, Blencowe NS, Boutron I et al. RoB 2: a revised tool for assessing risk of bias in randomised trials. BMJ. 2019 Aug 28;366:l4898. doi: 10.1136/bmj.l4898.
Kirmayr M, Quilodrán C, Valente B, Loezar C, Garegnani L, Franco JVA. The GRADE approach, Part 1: how to assess the certainty of the evidence. Medwave. 2021 Mar 17;21(2):e8109. Spanish, English. doi: 10.5867/medwave.2021.02.8109
