
Versión 1 - 27/03/2023
En pacientes sometidos a cirugía cardiaca, los niveles de elevación perioperatorios de troponina I de alta sensibilidad (hs-TnI) se asocian progresivamente a mayor riesgo de muerte o complicaciones vasculares mayores en el primer mes de la intervención. Además, añadir esta información al EuroSCORE II aumenta levemente su capacidad predictiva. Aunque no se han establecido con precisión los umbrales asociados a mayor tasa de complicaciones, se sugiere la medición y monitoreo de este biomarcador para estratificar el riesgo en esta población.
Certeza en la evidencia: moderada por imprecisión en los umbrales de hs-TnI asociados a las categorías de riesgo.
Otros mensajes clave:
Los valores de hs-TnI para injuria miocárdica fueron derivados en el estudio reseñado por su asociación con el riesgo de eventos y difieren de los descritos en la literatura.
Es importante saber lo que no se conoce:
* Se desconoce la asociación entre la hs-TnI y los resultados clínicos a largo plazo (ej. incidencia de falla cardiaca).
* No se conoce si existe un efecto diferencial para el aumento de los niveles de hs-TnI en subgrupos de pacientes, técnicas quirúrgicas o tipos de procedimientos.
* Se desconoce la eficacia de intervenciones específicas que en presencia de hs-TnI puedan reducir los desenlaces cardiovasculares adversos en el corto y largo plazo, adicionales a las del cuidado perioperatorio cardiovascular convencional.
Otros mensajes clave:
Los valores de hs-TnI para injuria miocárdica fueron derivados en el estudio reseñado por su asociación con el riesgo de eventos y difieren de los descritos en la literatura.
Es importante saber lo que no se conoce:
* Se desconoce la asociación entre la hs-TnI y los resultados clínicos a largo plazo (ej. incidencia de falla cardiaca).
* No se conoce si existe un efecto diferencial para el aumento de los niveles de hs-TnI en subgrupos de pacientes, técnicas quirúrgicas o tipos de procedimientos.
* Se desconoce la eficacia de intervenciones específicas que en presencia de hs-TnI puedan reducir los desenlaces cardiovasculares adversos en el corto y largo plazo, adicionales a las del cuidado perioperatorio cardiovascular convencional.
Antecedentes
Dentro de las opciones de tratamiento para la enfermedad coronaria obstructiva y las valvulopatías cardiacas se incluyen las terapias farmacológicas y/o invasivas, siendo estás últimas las destinadas para enfermedades más complejas, no susceptibles de terapia medica óptima, y que corresponden a intervenciones percutáneas (angioplastia + stent coronario, valvuloplastia, reemplazo valvular, etc.) o de cirugía cardiaca.
Los procedimientos de revascularización miocárdica (CABG, por sus siglas en inglés) y reparación/reemplazo valvular con prótesis (1,2) son tratamientos de elección, practicados ampliamente. Existe una relación entre los recursos disponibles y el volumen de cirugía practicado y de este, con sus resultados y complicaciones: mientras en países como Reino Unido se efectuaron (para 2016/2019) cerca de 34000 cirugías cardiacas al año (3), en toda Latinoamérica en 2010 se realizaron 22500 (4). Para el primer escenario, se estimó una tasa de mortalidad asociada de 2.59%, siendo del 1% para procedimientos electivos (3). En contraste, se desconocen las cifras regionales o nacionales sobre mortalidad o complicaciones asociadas.
Por su naturaleza, la cirugía cardiaca conlleva, a pesar de sus avances, alto riesgo de complicaciones (5) y reingresos (6). Para identificar estos riesgos y planear estrategias de mitigación (7-10) se utilizan ampliamente escalas válidas de predicción (11-13). Además, con la disponibilidad de la medición de troponinas, se ha identificado la “injuria miocárdica” , que en el escenario de cirugía no cardiaca se conoce como MINS (del inglés myocardial injury in noncardiac surgery) (14,15). En cirugía cardiaca (específicamente en CABG), donde también se ha utilizado recientemente el término “injuria miocárdica” se conoce de tiempo atrás el término “infarto miocárdico tipo 5” que representa la adición de síntomas y/o signos de isquemia aguda a la injuria miocárdica.
En procedimientos en los que se manipula el miocardio, ha sido un reto definir los umbrales de diagnóstico para injuria e infarto miocárdicos. Se han propuesto puntos de corte para infarto miocárdico que aplican exclusivamente a las estrategias de reperfusión percutánea o quirúrgica, identificándose para ésta última, umbrales de 10 (16) y 35 o más veces el límite superior de referencia (LSR) del percentil 99 del escenario no perioperatorio. Para “injuria miocárdica peri procedimental significativa”, estos niveles deben superar 70 veces el LSR (17) Asimismo, permanecen interrogantes sobre los puntos de corte para troponinas T e I de alta sensibilidad, toda vez que la evidencia muestra diferencias en la cinética de sus niveles (18).
Al igual que en cirugía no cardiaca (14,15), los estudios de injuria miocárdica en cirugía cardiaca indican consistentemente una fuerte asociación entre la elevación de troponinas y la presentación de eventos clínicos adversos (Ej. En CABG, la elevación de 100-400 veces el LSR de TnI convencional incrementa 3.61 veces el riesgo de muerte a 30 días, IC95%: 1.08-12.04) (19-23). Sin embargo, en cirugía cardiaca, no se han identificado intervenciones efectivas, como ocurre para MINS con dabigatrán (24).
Este Recado reseña un estudio reciente y de gran tamaño (25) sobre el valor pronóstico de hs-TnI y su potencial rol en la delimitación de nuevos puntos de corte para injuria miocárdica en cirugía cardiaca.
Información en la que se basa este Recado
Por interés en el tema, luego de monitoreo sistemático de repositorios de información, se identificó el estudio VISION Cirugía Cardiaca (2018) (27), estudio de cohorte prospectivo internacional en pacientes ≥18 años sometidos a estos procedimientos entre mayo de 2013 y abril de 2019. Se excluyeron aquellos llevados a procedimientos menores (ventana pericárdica aislada, pericardiectomía, implantación de un marcapasos o desfibrilador), con infarto de miocardio preoperatorio el mismo día o el día antes de su cirugía o los que tenían una hs-TnI ≥300 ng/L dentro de las 12h previas al procedimiento.
Los pacientes se seleccionaron a través de un muestreo por conveniencia y se recolectaron datos sobre posibles predictores de complicaciones perioperatorias, incluyendo los componentes del Sistema Europeo de Evaluación del Riesgo Quirúrgico Cardíaco II (EuroSCORE II).
Las muestras para la medición de la hs-TnI (Abbott ARCHITECT, P99: 26 ng/L, límite de detección: 1-2 n/L) fueron obtenidas antes de la cirugía y en el posoperatorio (3-12h, días 1, 2 y 3). Los pacientes, recolectores de datos y el personal asistencial desconocían los resultados de estas pruebas.
El desenlace primario fue muerte a 30 días después de la intervención. El secundario fue un compuesto de eventos o “complicación vascular mayor” (combinación de muerte por complicación vascular a 30 días, infarto de miocardio entre el día 4 al 30, o inserción de dispositivo de asistencia mecánica durante la estancia del paciente en UCI posquirúrgica).
Resultados
Entre los 15984 pacientes registrados en VISION cirugía cardíaca, se incluyeron 13862 para este análisis (97.2% con datos de mortalidad a 30 días). El promedio de edad fue de 63.3 años, 70.9% hombres, 29.3% con antecedente de infarto de miocardio, 66% de hipertensión y 16.3% de falla cardiaca. Las proporciones de los pacientes llevados a CABG, reemplazo valvular aórtico (AVR, por sus siglas en inglés) aislado y otras cirugías fueron 46.9%, 12.5% y 40.6% respectivamente. La puntuación media en el EuroSCORE II fue de 2.4%. La mediana de mediciones de hs-TnI posoperatorias fue de 4 (RIC 3-4) por paciente.
A continuación, se presentan los principales resultados:
- A los 30 días después de la cirugía, 296 pacientes (2.1%) habían fallecido y 399 pacientes (2.9%) habían tenido una complicación vascular mayor.
- El promedio general de hs-TnI preoperatoria fue de 9 ng/L (RIC 4-20) y la mediana del pico individual de hs-TnI fue 3920 ng/L (RIC 1799-8734).
- De acuerdo con el LSR para el ámbito no perioperatorio (26 ng/L), la distribución de los valores máximos del biomarcador en el primer día posoperatorio fue:
- >10 veces el LSR (260 ng/L) en el 97.5% de los participantes
- ≥35 veces el LSR (910 ng/L) en el 89.4% de los participantes
- ≥70 veces el LSR (1820 ng/L) en el 74.7% de los participantes
- Se encontró una relación positiva y continua entre el pico postoperatorio de la hs-Tnl y la mortalidad, tanto en el día 1 como en los días 2-3 posoperatorios. Esta relación se mantuvo después de ajustar por EuroSCORE II en un análisis multivariado por el logaritmo del pico de hs-TnI en el día 1 posoperatorio en CABG o AVR (aHR 1.62, IC95% 1.36-1.93) y para los otros procedimientos (aHR 1.75, IC95% 1.48-2.07). Estos resultados fueron consistentes en el día 2-3 (tabla 1).

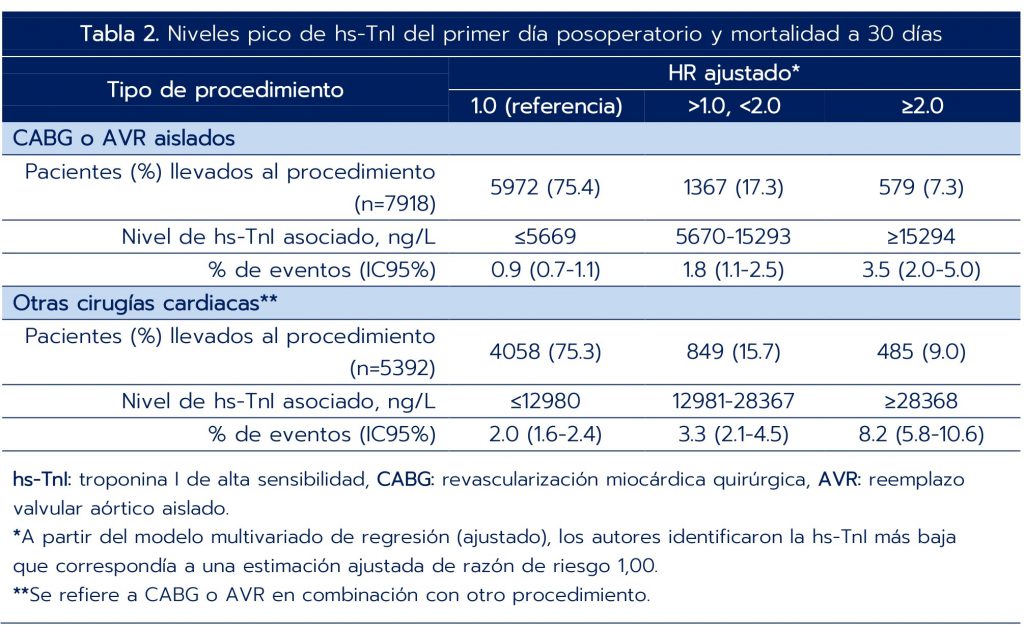
- Para los dos grupos de procedimientos, se clasificó la población de acuerdo con los niveles pico de hs-TnI en el día 1 asociados al riesgo ajustado de mortalidad (aHR=1 como referencia; 1-2 o >2), encontrando una mortalidad progresivamente mayor (0.9, 1.8 y 3.5%) para los tres niveles de riesgo. Para los otros procedimientos, siguiendo el mismo análisis, la mortalidad fue de 2, 3.3 y 8.2%, en las tres categorías de riesgo (tabla 2).
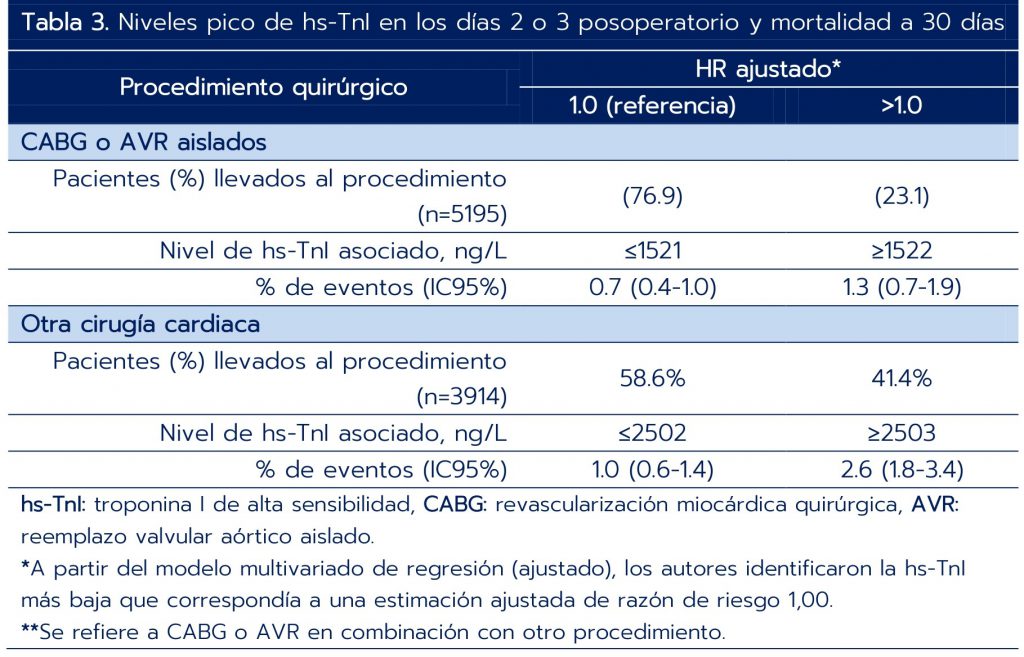
- En los días 2-3 para los procedimientos de CABG y AVR se encontró que a partir de 1522 ng/L de hs-TnI (23.1% de la población) el riesgo de muerte empieza a ser superior a 1 y para los otros procedimientos se empieza a generar el riesgo a partir de 2503 ng/L (41.4%% de la población) (tabla 3).
- Para la complicación cardiovascular mayor los umbrales del biomarcador fueron:
CABG y AVR:
– Para el día 1 posoperatorio: 161 veces el LSR (4184 ng/L)
– Para los días 2-3 posoperatorios: 42 veces el LSR (1099 ng/L)
Otros procedimientos:
– Para el día 1 posoperatorio: 371 veces el LSR (9654 ng/L)
– Para los días 2-3 posoperatorios: 73 veces el LSR (1888 ng/L)
- En términos de área bajo la curva, se encontró que al agregar los niveles de troponina pico al EuroSCORE II la predicción de la mortalidad a 30 días pasó de 0.69 a 0.74 (día 1) y de 0.80 a 0.83 (días 2-3).
- No se reportaron umbrales para lesión miocárdica debida a isquemia (por ejemplo, trombosis coronaria aguda) o injuria miocárdica cardíaca por otras causas (ej. reperfusión, lesión o trauma quirúrgico).
- No se exploró el efecto de diferentes técnicas y procedimientos empleados en cirugía cardiaca (anestesia, ventilación mecánica, circulación extracorpórea, protección miocárdica, soporte transfusional, etc.) en los niveles de hs-TnI y los desenlaces de interés.
Información sobre la evidencia que soporta este Recado
La aplicación de la herramienta QUIPSS (26), dirigida a estudios de factores pronóstico, permite concluir bajo riesgo de sesgos. Por otra parte, siguiendo la metodología GRADE para el mismo escenario (27) la certeza global en la evidencia para muerte a 30 días se consideró moderada. En la calificación de certeza se disminuyó dos niveles por imprecisión en la tasa de eventos (en las categorías de mayor riesgo) y los umbrales de referencia de hs-TnI. Se aumentó la calificación por el gradiente ascendente entre los niveles del biomarcador y el riesgo del evento (Ver tabla GRADE).
Referencias
Writing Committee Members; Lawton JS, Tamis-Holland JE, Bangalore S, Bates ER, Beckie TM, Bischoff JM, et al.. 2021 ACC/AHA/SCAI Guideline for Coronary Artery Revascularization: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol. 2022 Jan 18;79(2):e21-e129. doi: 10.1016/j.jacc.2021.09.006
Vahanian A, Beyersdorf F, Praz F, Milojevic M, Baldus S, Bauersachs J et al; ESC/EACTS Scientific Document Group. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J. 2022 Feb 12;43(7):561-632. doi: 10.1093/eurheartj/ehab395.
National Adult Cardiac Surgery Audit (NACSA) 2020 Summary Report (2016/17-2018/19 data). Available at:https://www.nicor.org.uk/adult-cardiac-surgery-surgery-audit/
Bertolotti A, Favaloro RR. Status and development of allied health personnel in cardiothoracic surgery in Latin America. HSR Proc Intensive Care Cardiovasc Anesth. 2011;3(4):263-8. PMID: 23440230; PMCID: PMC3563441.
Ball L, Costantino F, Pelosi P. Postoperative complications of patients undergoing cardiac surgery. Curr Opin Crit Care. 2016 Aug;22(4):386-92. doi: 10.1097/MCC.0000000000000319. PMID: 27309972.
Shawon MSR, Odutola M, Falster MO, Jorm LR. Patient and hospital factors associated with 30-day readmissions after coronary artery bypass graft (CABG) surgery: a systematic review and meta-analysis. J Cardiothorac Surg. 2021 Jun 10;16(1):172. doi: 10.1186/s13019-021-01556-1. PMID: 34112216; PMCID: PMC8194115.
Aya HD, Cecconi M, Hamilton M, Rhodes A. Goal-directed therapy in cardiac surgery: a systematic review and meta-analysis. Br J Anaesth. 2013 Apr;110(4):510-7. doi: 10.1093/bja/aet020. Epub 2013 Feb 27. PMID: 23447502.
Engelman DT, Ben Ali W, Williams JB, Perrault LP, Reddy VS, Arora RC et al. Guidelines for Perioperative Care in Cardiac Surgery: Enhanced Recovery After Surgery Society Recommendations. JAMA Surg. 2019 Aug 1;154(8):755-766. doi: 10.1001/jamasurg.2019.1153
Pajares MA, Margarit JA, García-Camacho C, García-Suarez J, Mateo E, Castaño M et al. Guidelines for enhanced recovery after cardiac surgery. Consensus document of Spanish Societies of Anesthesia (SEDAR), Cardiovascular Surgery (SECCE) and Perfusionists (AEP). Rev Esp Anestesiol Reanim (Engl Ed). 2021 Apr;68(4):183-231. English, Spanish. doi: 10.1016/j.redar.2020.11.005
Accini Mendoza JL, Atehortua L LH, Nieto Estrada VH, Rebolledo M CE, Duran Pérez JC, Senior JM et al. Consenso colombiano de cuidados perioperatorios en cirugía cardiaca del paciente adulto. 1 de abril de 2020;20(2):118-57. Disponible en: https://doi.org/10.1016/j.acci.2020.03.002
Sanders J, Makariou N, Tocock A, Magboo R, Thomas A, Aitken LM. Preoperative risk assessment tools for morbidity after cardiac surgery: a systematic review. Eur J Cardiovasc Nurs. 2022 Oct 14;21(7):655-664. doi: 10.1093/eurjcn/zvac003. PMID: 35171231.
Sullivan PG, Wallach JD, Ioannidis JP. Meta-Analysis Comparing Established Risk Prediction Models (EuroSCORE II, STS Score, and ACEF Score) for Perioperative Mortality During Cardiac Surgery. Am J Cardiol. 2016 Nov 15;118(10):1574-1582. doi: 10.1016/j.amjcard.2016.08.024
Petäjä L, Røsjø H, Mildh L, Suojaranta-Ylinen R, Kaukonen KM, Jokinen JJ et al. Predictive value of high-sensitivity troponin T in addition to EuroSCORE II in cardiac surgery. Interact Cardiovasc Thorac Surg. 2016 Jul;23(1):133-41. doi: 10.1093/icvts/ivw060.
Vascular Events in Noncardiac Surgery Patients Cohort Evaluation (VISION) Study Investigators; Spence J, LeManach Y, Chan MTV, Wang CY, Sigamani A, Xavier D et al. Association between complications and death within 30 days after noncardiac surgery. CMAJ. 2019 Jul 29;191(30):E830-E837. doi: 10.1503/cmaj.190221.
Ruetzler K, Smilowitz NR, Berger JS, Devereaux PJ, Maron BA, Newby LK et al. Diagnosis and Management of Patients With Myocardial Injury After Noncardiac Surgery: A Scientific Statement From the American Heart Association. Circulation. 2021 Nov 9;144(19):e287-e305. doi: 10.1161/CIR.0000000000001024.
Thygesen K, Alpert JS, Jaffe AS, Chaitman BR, Bax JJ, Morrow DA, White HD; Executive Group on behalf of the Joint European Society of Cardiology (ESC)/American College of Cardiology (ACC)/American Heart Association (AHA)/World Heart Federation (WHF) Task Force for the Universal Definition of Myocardial Infarction. Fourth Universal Definition of Myocardial Infarction (2018). J Am Coll Cardiol. 2018 Oct 30;72(18):2231-2264. doi: 10.1016/j.jacc.2018.08.1038.
Garcia-Garcia HM, McFadden EP, Farb A, Mehran R, Stone GW, Spertus J et al; Academic Research Consortium. Standardized End Point Definitions for Coronary Intervention Trials: The Academic Research Consortium-2 Consensus Document. Circulation. 2018 Jun 12;137(24):2635-2650. doi: 10.1161/CIRCULATIONAHA.117.029289
Denessen EJ, Heuts S, Daemen JH, van Doorn WP, Vroemen WH, Sels JW et al. High-Sensitivity Cardiac Troponin I and T Kinetics Differ following Coronary Bypass Surgery: A Systematic Review and Meta-Analysis. Clin Chem. 2022 Dec 6;68(12):1564-1575. doi: 10.1093/clinchem/hvac152.
Domanski MJ, Mahaffey K, Hasselblad V, Brener SJ, Smith PK, Hillis G et al. Association of myocardial enzyme elevation and survival following coronary artery bypass graft surgery. JAMA. 2011 Feb 9;305(6):585-91. doi: 10.1001/jama.2011.99. PMID: 21304084.
Lurati Buse GA, Koller MT, Grapow M, Bolliger D, Seeberger M, Filipovic M. The prognostic value of troponin release after adult cardiac surgery - a meta-analysis. Eur J Cardiothorac Surg. 2010 Feb;37(2):399-406. doi: 10.1016/j.ejcts.2009.05.054
Tevaearai Stahel HT, Do PD, Klaus JB, Gahl B, Locca D, Göber V, Carrel TP. Clinical Relevance of Troponin T Profile Following Cardiac Surgery. Front Cardiovasc Med. 2018 Dec 13;5:182. doi: 10.3389/fcvm.2018.00182.
Omran H, Deutsch MA, Groezinger E, Zittermann A, Renner A, Neumann JT et al. High-sensitivity cardiac troponin I after coronary artery bypass grafting for post-operative decision-making. Eur Heart J. 2022 Jul 1;43(25):2388-2403. doi: 10.1093/eurheartj/ehab918
Ahmed SH, Pervez N, Rehan ST, Shaikh TG, Waseem S. Postoperative cardiac troponin I as an indicator of surgical outcomes: A systematic review. J Card Surg. 2022 Dec;37(12):5351-5361. doi: 10.1111/jocs.17197.
Devereaux PJ, Duceppe E, Guyatt G, Tandon V, Rodseth R, Biccard BM et al; MANAGE Investigators. Dabigatran in patients with myocardial injury after non-cardiac surgery (MANAGE): an international, randomised, placebo-controlled trial. Lancet. 2018 Jun 9;391(10137):2325-2334. doi: 10.1016/S0140-6736(18)30832-8.
Devereaux PJ, Lamy A, Chan MTV, Allard RV, Lomivorotov VV, Landoni G et al; VISION Cardiac Surgery Investigators. High-Sensitivity Troponin I after Cardiac Surgery and 30-Day Mortality. N Engl J Med. 2022 Mar 3;386(9):827-836. doi: 10.1056/NEJMoa2000803.
Hayden JA, van der Windt DA, Cartwright JL, Côté P, Bombardier C. Assessing bias in studies of prognostic factors. Ann Intern Med. 2013 Feb 19;158(4):280-6. doi: 10.7326/0003-4819-158-4-201302190-00009. PMID: 23420236.
Foroutan F, Guyatt G, Zuk V, Vandvik PO, Alba AC, Mustafa R et al. GRADE Guidelines 28: Use of GRADE for the assessment of evidence about prognostic factors: rating certainty in identification of groups of patients with different absolute risks. J Clin Epidemiol. 2020 May;121:62-70. doi: 10.1016/j.jclinepi.2019.12.023.
