1 - 15/09/2024
En adultos llevados a trasplante hepático, el ultrasonido Doppler con contraste* muestra un rendimiento diagnóstico favorable para detectar oclusión de la arteria hepática (de 40 casos en 1000 pacientes: 1 falso negativo y 9 falsos positivos) cuando se compara con angio-tomografía, angio-resonancia o angiografía. Este estudio podría ser una herramienta diagnóstica complementaria al ultrasonido Doppler convencional cuando sus resultados no son concluyentes. Sin embargo, su uso está condicionado a la disponibilidad y costos locales.
-
*Microburbujas de hexafluoruro de azufre, perflutreno o galactosa con ácido palmítico.
Certeza en la evidencia: moderada por riesgo serio de sesgos ⨁⨁⨁◯.
Otro mensaje clave
- La capacidad de discriminación del ultrasonido Doppler con contraste es alta (área bajo la curva ROC: 0.959).
Es importante saber lo que no se conoce:
- No se conoce el desempeño del ultrasonido Doppler con contraste en poblaciones diferentes a norteamericana, asiática y europea.
- Se desconoce la costo-efectividad de la técnica a largo plazo
Antecedentes
Las enfermedades hepáticas crónicas (EHC) representan una carga significativa a nivel mundial, contribuyendo a aproximadamente 2 millones de muertes al año (1). Las principales causas incluyen la cirrosis, predominantemente por hepatitis C, con una prevalencia mundial del 25-30%, y la enfermedad hepática alcohólica, que afecta al 20-25% de los pacientes (2,3). Además, la enfermedad hepática grasa no alcohólica afecta al 15-20% de la población, mientras que la colangitis esclerosante primaria y el carcinoma hepatocelular tienen una prevalencia cercana al 10% (4,5).
En Colombia, la cirrosis y el carcinoma hepatocelular son prevalentes, reflejando patrones similares a nivel global, siendo la cirrosis hepática la principal causa de trasplante hepático (6). Las complicaciones más comunes de las EHC incluyen la insuficiencia hepática, la hipertensión portal y el carcinoma hepatocelular, siendo el trasplante hepático la única opción curativa en estadios terminales (7).
Anualmente, se realizan alrededor de 35,000 trasplantes hepáticos (TH) a nivel mundial, con Estados Unidos y Europa liderando en número de procedimientos (8). En Colombia, se efectuaron 208 TH en 2021, siendo la Fundación Cardio infantil la institución que realizó el 17.5% de los procedimientos de donante fallecido y el 72% de donante vivo (6). Las cifras de TH a nivel nacional han venido aumentando dada la realización de 293 procedimientos para 2023 (9).
A pesar de sus beneficios, las complicaciones postrasplantes, como la trombosis de la arteria hepática (TAH), afectan entre el 4% y el 12% de los receptores, siendo una de las principales causas de pérdida del injerto (10). Otras complicaciones incluyen el rechazo agudo y las infecciones, que pueden llevar al fracaso del injerto. La sobrevida a un año es del 85-90%, mientras que a cinco años se reduce al 70-75% (10).
En este contexto, el ultrasonido Doppler (USD) es una herramienta esencial para la detección temprana de TAH, permitiendo una evaluación en tiempo real de la perfusión hepática. Su rendimiento diagnóstico es variable, con cifras de sensibilidad reportadas entre 70-90% y especificidad entre 90-95%, dependiendo de la experiencia del operador y la calidad del equipo. Aunque es una técnica no invasiva y de bajo costo, su rendimiento puede ser subóptimo en algunos casos debido a limitaciones como la obesidad del paciente y la presencia de gas intestinal (11).
Existen técnicas complementarias al USD como la tomografía computarizada (TC) y la resonancia magnética (RM), con mejor desempeño diagnóstico dados valores de sensibilidad y especificidad del 95 y 98% (12) para la primera y 92% y 97% para la segunda (13). No obstante, se resaltan como limitaciones la exposición a la radiación y el uso de medio de contraste iodado para la CTA y la inmovilidad prolongada, uso de gadolinio, reducida disponibilidad y altos costos de la MRA.
El ultrasonido con contraste (USCC) ha emergido como una alternativa eficaz (14,15) y segura (tasa de efectos adversos del contraste < 1%) (16-18) para la detección de complicaciones vasculares. La técnica emplea microburbujas de contraste para mejorar la visualización del flujo sanguíneo y la perfusión hepática (19, 20). El recado explora la evidencia sobre el rendimiento diagnóstico de esta técnica para la oclusión de la arteria hepática (EAH) en pacientes trasplantados.
Información en la que se basa este Recado
La estrategia de búsqueda (hasta el 30 de junio de 2024) incluyó los términos “contrast-enhanced ultrasound/CEUS”, “microbubbles”, “hepatic artery occlusion/HAO”, “hepatic artery stenosis/HAS”, “hepatic artery thrombosis/HAT”, “liver transplantation” en las bases de datos Medline/Pubmed, Embase, Cochrane. Luego de filtrar para revisiones sistemáticas (RS) se recuperaron los estudios de Chen et al (15) y Songtanin et al (21), de los cuales se seleccionó el último dada su vigencia.
La RS con metaanálisis (21) incluyó estudios que evaluaron a la población adulta, excluyendo series de casos, informes de casos y publicaciones en otros idiomas si los datos no eran accesibles.
Se recopiló información sobre las características del estudio y la población, incluidos el número de pacientes, edad, género, tipo de trasplante y duración del seguimiento. Además, se evaluaron criterios de diagnóstico para USCC, estándar de referencia (angio-tomografía, angio-resonancia, angiografía), prevalencias de obstrucción de la arteria hepática (OAH), estenosis de la arteria hepática (EAH) y trombosis de la arteria hepática (TAH), así como sensibilidad y especificidad. La evaluación de la calidad de los estudios primarios se realizó con el instrumento QUADAS-2.
En el análisis estadístico se calcularon la sensibilidad y especificidad agrupadas, el log de la razón de probabilidad diagnóstica (LDOR) y el área bajo la curva ROC (AUROC). También se evaluó el sesgo de publicación con el diagrama de embudo de Deeks y pruebas de asimetría.
Resultados
A continuación, se resumen las características de los estudios incluidos en el metaanálisis (Anexo 1):
- Se incluyeron ocho estudios en el metaanálisis, con un total de 434 exámenes USCC realizados en 1145 pacientes trasplantados.
- La edad promedio de los participantes fue variada entre los estudios (46-53 años). La proporción de mujeres también fue heterogénea (20-62%).
- La mayoría de los trasplantes (69%) fueron de donante fallecido, mientras que otros tipos incluyeron donante vivo, dominó*, retrasplantes, injertos divididos y autotrasplantes.
- Los criterios de diagnóstico para OAT en USCC incluyeron la ausencia de flujo arterial y la forma de onda parvus tardus.
* Trasplante domino: Es un tipo de trasplante en el que un receptor de un trasplante de hígado, cuyo propio hígado no es saludable, pero puede ser útil para otro paciente, dona su hígado a otro receptor.
La tabla 1 presenta el rendimiento del USCC para detectar EAH. El análisis global muestra valores de sensibilidad y especificidad agrupadas de 0.969 (IC95% 0.938-0.996) y 0.991 (IC95% 0.981-1.001) respectivamente.
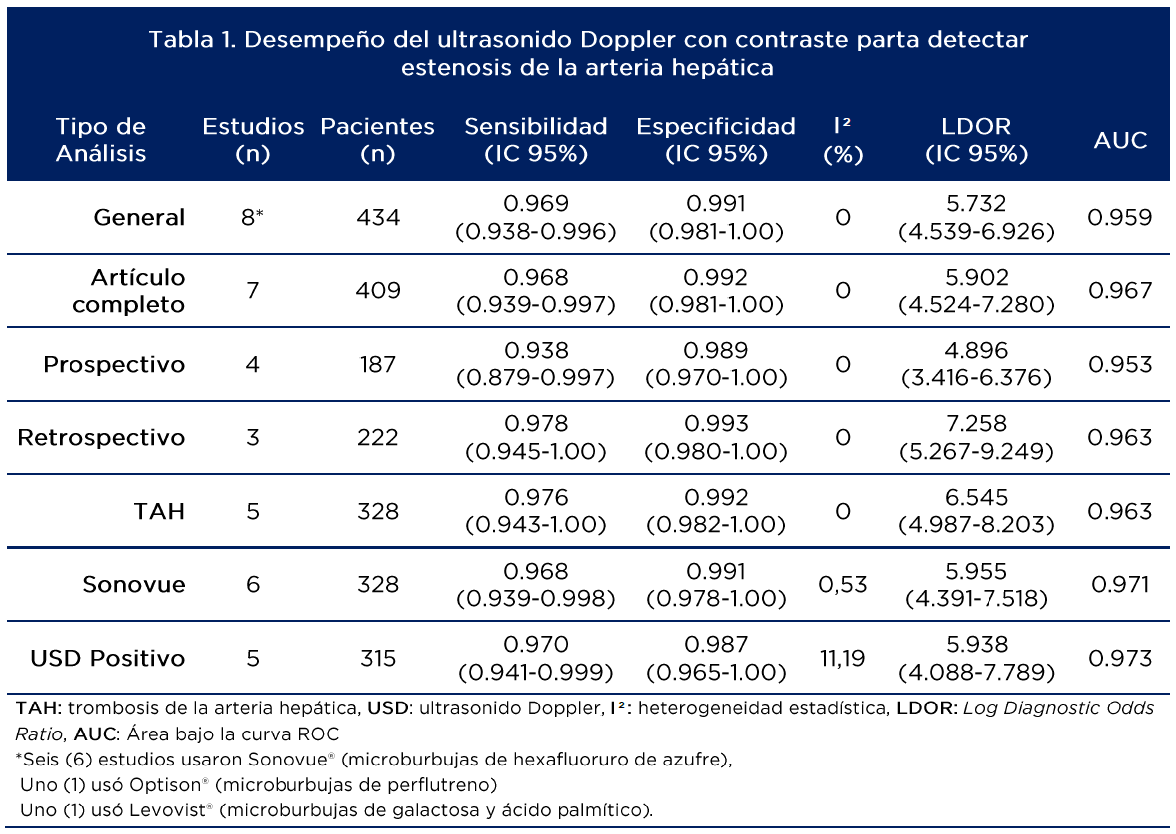
En otros hallazgos:
- El LDOR fue de 5.732 (IC95% 4.539-6.926) y el AUROC fue de 0.959, indicando un rendimiento diagnóstico satisfactorio. La heterogeneidad entre los estudios fue baja y no se encontró sesgo de publicación (p=0.44).
- Los análisis de subgrupos mostraron que no hubo diferencias en sensibilidad y especificidad según el tipo de publicación y estudio.
- El análisis de sensibilidad demostró que el rendimiento de USCC fue similar, independientemente del tipo de EAH, el tipo de contraste usado, y la indicación de realizar USCC tras un USD positivo.
Los resultados indican que el USCC es una modalidad altamente efectiva para la detección de EAO en pacientes postrasplante, proporcionando una alternativa viable cuando el USD no es diagnóstico o cuando las modalidades más invasivas no son factibles.
Nota metodológica:
El DOR, del inglés “diagnostic odds ratio” representa la relación entre la probabilidad de que la prueba sea positiva en individuos con la enfermedad y la probabilidad de que la prueba sea positiva en individuos sin la enfermedad. Proporciona una medida única y global del rendimiento de una prueba diagnóstica. Un DOR mayor que 1 indica que la prueba es efectiva para distinguir entre individuos con y sin la enfermedad. Un DOR igual a 1 indica que la prueba no tiene capacidad discriminativa (22).
El LDOR, del inglés «logarithm of the diagnostic odds ratio» es simplemente el logaritmo natural del DOR. Se utiliza en metaanálisis para combinar resultados de diversos estudios y permite comparar la precisión diagnóstica de diferentes pruebas de manera menos susceptible a valores extremos que el DOR. Un LDOR más alto indica un mejor rendimiento de la prueba, mientras que un LDOR de 0 sugiere que la prueba no tiene capacidad discriminativa (23).
Información sobre la evidencia que soporta este recado
Luego de aplicar la herramienta de evaluación crítica AMSTAR-2 (24) se concluyó confianza baja (protocolo no registrado) en la revisión sistemática (Anexo 2).
Aunque los autores de la RS concluyeron bajo riesgo de sesgos partir del instrumento QUADAS-2 (25), resaltan que, en un estudio, la prueba índice, el estándar de referencia y el flujo no fueron claros. Asimismo, en cinco estudios no mencionaron si los resultados de las pruebas del estándar de referencia fueron interpretados con o sin conocimiento de la prueba índice. Por las preocupaciones descritas, los autores del recado consideran riesgo alto de sesgos.
La certeza global en la evidencia a partir de la metodología GRADE (26,27) se concluyó moderada por cuenta de riesgo serio de sesgos (Anexo 3).
Unidad de Síntesis y Transferencia de Conocimiento | Correspondencia: jvillarc@lacardio.org
Rodríguez, J*; Villar J**; Moreno, K**; Cruz, J**; Balcázar M**+
(*)Desarrollo, (**)Edición, (+)Diseminación
¿Tienes una pregunta clínica que nuestra Unidad de Síntesis y Transferencia del Conocimiento pueda resolver a través de evidencia científica?
Sí, enviar pregunta
Referencias
Asrani SK, Devarbhavi H, Eaton J, Kamath PS. Burden of liver diseases in the world. J Hepatol. 2019;70(1):151-171. doi: 10.1016/j.jhep.2018.09.014.
European Association for the Study of the Liver. EASL Clinical Practice Guidelines: Liver transplantation. J Hepatol. 2016;64(2):433-485. doi: 10.1016/j.jhep.2015.10.006.
Global Burden of Disease Liver Cancer Collaboration. The burden of primary liver cancer and underlying etiologies. JAMA Oncol. 2017;3(12):1683-1691. doi:10.1001/jamaoncol.2017.3055.
Younossi ZM, Koenig AB, Abdelatif D, Fazel Y, Henry L, Wymer M. Global epidemiology of NAFLD-related HCC: trends, forecast and clinical implications. Hepatology. 2018;68(1):267-276. doi:10.1002/hep.29433.
Kim WR, Lake JR, Smith JM, et al. OPTN/SRTR 2018 Annual Data Report: Liver. Am J Transplant. 2020;20 Suppl 1:193-299. doi:10.1111/ajt.15671.
Instituto Nacional de Salud. Informe Anual Red de Donación y Trasplantes 2021. Consultado Julio 1 de 2024. Disponible en: [https://www.ins.gov.co/BibliotecaDigital/informe-anual-red-de-donacion-y-trasplantes-2021.pdf]
Instituto Nacional de Salud. Trasplantes en Colombia aumentaron un 17, 1%. Consultado: Julio 1 de 2024. Disponible en: [https://www.ins.gov.co/Noticias/Paginas/Trasplantes-en-Colombia-aumentaron.aspx]
United Network for Organ Sharing (UNOS). Annual Report 2021. Disponible en: [https://unos.org/data/transplant-trends/](https://unos.org/data/transplant-trends/)
Bekker J, Ploem S, de Jong KP. Early hepatic artery thrombosis after liver transplantation: a systematic review of the incidence, outcome and risk factors. Transplantation. 2009;87(6):889-896. doi:10.1097/TP.0b013e31819e4d95.
Adam R, Karam V, Delvart V, et al. Evolution of indications and results of liver transplantation in Europe. Semin Liver Dis. 2009;29(1):14-25. doi:10.1055/s-0028-1128153.
Brass CA, Ream RS, Al-Khafaji A, Yadav D. The use of Doppler ultrasound in liver transplantation. Liver Transpl. 2001;7(5):442-450. doi:10.1053/jlts.2001.23745.
Bieze M, van den Esschert JW, Olde Damink SW, et al. Diagnostic accuracy of computed tomography angiography in the assessment of hepatic artery complications after liver transplantation. Transpl Int. 2012;25(3):325-332. doi:10.1111/j.1432-2277.2011.01406. x.
Segev DL, Muaddi M, Syed L, et al. Magnetic resonance angiography in the evaluation of hepatic artery thrombosis after liver transplantation. Liver Transpl. 2009;15(5):592-598. doi:10.1002/lt.21714.
Kim JS, Kim KW, Choi SH, Jeong SY, Kwon JH, Song GW, Lee SG. Hepatic Artery Occlusion after Liver Transplantation in Patients with Doppler Ultrasound Abnormality: Increasing Sensitivity of Contrast-Enhanced Ultrasound Diagnosis. Korean J Radiol. 2019 Mar;20(3):459-468. doi: 10.3348/kjr.2018.0464.
Chen S, Wang X, Zhang B, Liu B, Pan H. Meta-analysis of the diagnostic value of contrast-enhanced ultrasound for the detection of vascular complications after liver transplantation. Rev Esp Enferm Dig. 2019 May;111(5):388-396. doi: 10.17235/reed.2018.5818/2018
Hauben, M., Hung, E., Hanretta, K., Bangalore, S., & Snow, V. (2015). Safety of Perflutren Ultrasound Contrast Agents: A Disproportionality Analysis of the US FAERS Database. Drug Safety, 38, 1127-1139. https://doi.org/10.1007/s40264-015-0332-6.
Tang C, Fang K, Guo Y, Li R, Fan X, Chen P, Chen Z, Liu Q, Zou Y. Safety of Sulfur Hexafluoride Microbubbles in Sonography of Abdominal and Superficial Organs: Retrospective Analysis of 30,222 Cases. J Ultrasound Med. 2017 Mar;36(3):531-538. doi: 10.7863/ultra.15.11075
Sencha AN, Patrunov YN, editors. General Aspects of the Use of Contrast Agents in Diagnostic Ultrasound. History and Current State of the Technology. Review of Contrast Agents. In: Sencha AN, Patrunov YN, editors. Contrast-Enhanced Ultrasound. Cham: Springer; 2022. https://doi.org/10.1007/978-3-030-91764-7_1
Wilson SR, Burns PN, Kono Y. The role of contrast-enhanced ultrasound in the assessment of focal liver lesions. Semin Roentgenol. 2016;51(4):337-352. doi:10.1053/j.ro.2016.07.006.
Porter TR, Feinstein SB, Senior R, Mulvagh SL, Nihoyannopoulos P, Strom JB et al. A CEUS cardiac exam protocols International Contrast Ultrasound Society (ICUS) recommendations. Echo Res Pract. 2022 Aug 23;9(1):7. doi: 10.1186/s44156-022-00008-3
Songtanin B, Brittan K, Sanchez S, Le M, Schmidt C, Ingviya T, Manatsathit W. Diagnostic performance of contrast-enhanced ultrasound in diagnosing hepatic artery occlusion after liver transplantation: A systematic review and meta-analysis. Clin Transplant. 2023 nov;37(11): e15070. doi: 10.1111/ctr.15070
Deeks JJ, Altman DG. Diagnostic tests 4: likelihood ratios. BMJ. 2004 jul 17;329(7458):168-9. doi: 10.1136/bmj.329.7458.168. PMID: 15258077; PMCID: PMC478236.
Schwarzer G, Carpenter JR, Rücker G. Meta-Analysis of Diagnostic Test Accuracy Studies. In: ¡Meta-Analysis with R. Use R! Springer, Cham. 2015. https://doi.org/10.1007/978-3-319-21416-0_9
Shea BJ, Reeves BC, Wells G, Thuku M, Hamel C, Moran J, Moher D, Tugwell P, Welch V, Kristjansson E, Henry DA. AMSTAR 2: a critical appraisal tool for systematic reviews that include randomised or non-randomised studies of healthcare interventions, or both. BMJ. 2017 Sep 21;358: j4008. doi: 10.1136/bmj. j4008
Whiting PF, Rutjes AW, Westwood ME, Mallett S, Deeks JJ, Reitsma JB, Leeflang MM, Sterne JA, Bossuyt PM; QUADAS-2 Group. QUADAS-2: a revised tool for the quality assessment of diagnostic accuracy studies. Ann Intern Med. 2011 oct 18;155(8):529-36. doi: 10.7326/0003-4819-155-8-201110180-00009
Schünemann HJ, Mustafa RA, Brozek J, Steingart KR, Leeflang M, Murad MH et al; GRADE Working Group. GRADE guidelines: 21 part 1. Study design, risk of bias, and indirectness in rating the certainty across a body of evidence for test accuracy. J Clin Epidemiol. 2020 jun; 122:129-141. doi: 10.1016/j.jclinepi.2019.12.020
Schünemann HJ, Mustafa RA, Brozek J, Steingart KR, Leeflang M, Murad MH, Bossuyt P et al; GRADE Working Group. GRADE guidelines: 21 part 2. Test accuracy: inconsistency, imprecision, publication bias, and other domains for rating the certainty of evidence and presenting it in evidence profiles and summary of findings tables. J Clin Epidemiol. 2020 jun; 122:142-152. doi: 10.1016/j.jclinepi.2019.12.021
